Группа Н09
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Дата введения 01.01.2012
Предисловие
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. N 184-ФЗ "О техническом регулировании", а правила применения национальных стандартов Российской Федерации - ГОСТ Р 1.0-2004 "Стандартизация в Российской Федерации. Основные положения"
Сведения о стандарте
1 ПОДГОТОВЛЕН Государственным научным учреждением Всероссийским научно-исследовательским институтом консервной и овощесушильной промышленности (ГНУ ВНИИКОП) на основе собственного аутентичного перевода на русский язык стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 93 "Продукты переработки фруктов, овощей и грибов"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 26 ноября 2010 г. N 542-ст
4 Настоящий стандарт идентичен европейскому региональному стандарту ЕН 14130:2003* "Продукты пищевые. Определение витамина С. Метод высокоэффективной жидкостной хроматографии" (EN 14130:2003 "Foodstuffs - Determination of vitamin C by HPLC").
* Доступ к международным и зарубежным документам, упомянутым здесь и далее по тексту, можно получить, перейдя по ссылке.
Наименование настоящего стандарта изменено относительно наименования указанного международного стандарта для приведения в соответствие с ГОСТ Р 1.5 (пункт 3.5).
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты Российской Федерации, сведения о которых приведены в дополнительном приложении ДА
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячно издаваемых информационных указателях "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
Сведения о стандарте
1 ПОДГОТОВЛЕН Государственным научным учреждением Всероссийским научно-исследовательским институтом консервной и овощесушильной промышленности (ГНУ ВНИИКОП) на основе собственного аутентичного перевода на русский язык стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 93 "Продукты переработки фруктов, овощей и грибов"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 26 ноября 2010 г. N 542-ст
4 Настоящий стандарт идентичен европейскому региональному стандарту ЕН 14130:2003* "Продукты пищевые. Определение витамина С. Метод высокоэффективной жидкостной хроматографии" (EN 14130:2003 "Foodstuffs - Determination of vitamin C by HPLC").
* Доступ к международным и зарубежным документам, упомянутым здесь и далее по тексту, можно получить, перейдя по ссылке.
Наименование настоящего стандарта изменено относительно наименования указанного международного стандарта для приведения в соответствие с ГОСТ Р 1.5 (пункт 3.5).
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты Российской Федерации, сведения о которых приведены в дополнительном приложении ДА
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячно издаваемых информационных указателях "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
1 Область применения
Настоящий стандарт распространяется на пищевые продукты и устанавливает метод определения витамина С с использованием высокоэффективной жидкостной хроматографии (ВЭЖХ). Содержание витамина С определяется в виде суммарного содержания L(+)-аскорбиновой и L(+)-дегидроаскорбиновой кислот.
2 Нормативные ссылки
В настоящем стандарте использована нормативная ссылка на следующий стандарт:
ЕН ИСО 3696 Вода для лабораторного анализа. Технические требования и методы испытаний (ИСО 3696:1987)
ЕН ИСО 3696 Вода для лабораторного анализа. Технические требования и методы испытаний (ИСО 3696:1987)
3 Сущность метода
Метод основан на экстракции витамина С из пробы раствором метафосфорной кислоты, последующем восстановлении L(+)-дегидроаскорбиновой кислоты до L(+)-аскорбиновой кислоты и определении общего содержания L(+)-аскорбиновой кислоты методом высокоэффективной жидкостной хроматографии (ВЭЖХ) со спектрофотометрическим детектированием при длине волны 265 нм [1], [2].
4 Реактивы
4.1 Общие положения
При проведении анализа, если не оговорены другие условия, используют только реактивы установленной аналитической чистоты для ВЭЖХ-анализа и воду не ниже первой степени чистоты по ЕН ИСО 3696 или воду, подвергнутую дополнительной дистилляции.
4.2 Реактивы и растворы
4.2.1 Кислота метафосфорная (НРО )
) .
.
4.2.2 Натрий фосфорнокислый трехзамещенный (тринатрийфосфат) с массовой долей  (Na
(Na PO
PO ·12Н
·12Н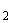 О)
О) 98,0%.
98,0%.
4.2.3 Калий фосфорнокислый однозамещенный с массовой долей (KH
(KH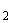 PO
PO )
) 98,0%.
98,0%.
4.2.4 L-цистеин с массовой долей (C
(C H
H NO
NO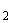 S)
S) 99,0% или другой приемлемый восстанавливающий реактив.
99,0% или другой приемлемый восстанавливающий реактив.
4.2.3 Калий фосфорнокислый однозамещенный с массовой долей
4.2.4 L-цистеин с массовой долей
4.2.5 N-цетил-N,N,N-триметиламмонийбромид (цетримид) с массовой долей  (C
(C H
H BrN)
BrN)  99,0%.
99,0%.
4.2.6 Метанол для ВЭЖХ с массовой долей (CH
(CH O)
O)  99,9%.
99,9%.
4.2.7 Раствор метафосфорной кислоты массовой концентрацией ((НРО
((НРО )
) )=200 г/дм
)=200 г/дм
200 г метафосфорной кислоты (см. 4.2.1) растворяют в воде в мерной колбе вместимостью 1 дм , объем содержимого доводят водой до метки. Срок годности раствора 1 мес при температуре 4 °С.
, объем содержимого доводят водой до метки. Срок годности раствора 1 мес при температуре 4 °С.
4.2.8 Раствор метафосфорной кислоты массовой концентрацией ((НРО
((НРО )
) )=20 г/дм
)=20 г/дм
50 см метафосфорной кислоты (см. 4.2.7) переносят пипеткой в мерную колбу вместимостью 500 см
метафосфорной кислоты (см. 4.2.7) переносят пипеткой в мерную колбу вместимостью 500 см , объем содержимого доводят водой до метки. Раствор готовят в день проведения анализа.
, объем содержимого доводят водой до метки. Раствор готовят в день проведения анализа.
4.2.9 Раствор натрия фосфорнокислого трехзамещенного массовой концентрацией (Na
(Na PO
PO ·12Н
·12Н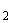 О)=200 г/дм
О)=200 г/дм
200 г тринатрийфосфата (см. 4.2.2) растворяют в воде в мерной колбе вместимостью 1 дм , объем содержимого доводят водой до метки.
, объем содержимого доводят водой до метки.
4.2.10 Раствор L-цистеина массовой концентрацией (C
(C H
H NO
NO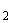 S)=40 г/дм
S)=40 г/дм
4.2.6 Метанол для ВЭЖХ с массовой долей
4.2.7 Раствор метафосфорной кислоты массовой концентрацией
200 г метафосфорной кислоты (см. 4.2.1) растворяют в воде в мерной колбе вместимостью 1 дм
4.2.8 Раствор метафосфорной кислоты массовой концентрацией
50 см
4.2.9 Раствор натрия фосфорнокислого трехзамещенного массовой концентрацией
200 г тринатрийфосфата (см. 4.2.2) растворяют в воде в мерной колбе вместимостью 1 дм
4.2.10 Раствор L-цистеина массовой концентрацией
20 г цистеина (см. 4.2.4) растворяют в воде в мерной колбе вместимостью 500 см , объем содержимого доводят водой до метки. Раствор готовят в день проведения анализа.
, объем содержимого доводят водой до метки. Раствор готовят в день проведения анализа.
4.2.11 Подвижная фаза для ВЭЖХ
Раствор А
4.2.11 Подвижная фаза для ВЭЖХ
Раствор А
13,6 г однозамещенного фосфата калия (см. 4.2.3) растворяют в стакане в 900 см воды. Раствор фильтруют через мембранный фильтр размером пор 0,45 мкм.
воды. Раствор фильтруют через мембранный фильтр размером пор 0,45 мкм.
Раствор В
100 см цетримида (см. 4.2.5) растворяют в стакане в 100 см
цетримида (см. 4.2.5) растворяют в стакане в 100 см метанола (см. 4.2.6). Раствор фильтруют через мембранный фильтр размером пор 0,45 мкм.
метанола (см. 4.2.6). Раствор фильтруют через мембранный фильтр размером пор 0,45 мкм.
Раствор В
100 см
Приготовленные растворы смешивают, используя 900 см раствора А и 100 см
раствора А и 100 см раствора В. Полученную подвижную фазу для ВЭЖХ при необходимости перед употреблением дегазируют.
раствора В. Полученную подвижную фазу для ВЭЖХ при необходимости перед употреблением дегазируют.
4.2.12 Крахмал (применяется по выбору пользователя), раствор массовой концентрацией 1 г/100 см .
.
4.2.13 Йод (применяется по выбору пользователя), раствор концентрацией (I
(I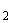 )=0,05 моль/дм
)=0,05 моль/дм .
.
4.2.14 Кислота серная, раствор концентрацией (H
(H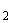 SO
SO )=0,1 моль/дм
)=0,1 моль/дм .
.
4.2.12 Крахмал (применяется по выбору пользователя), раствор массовой концентрацией 1 г/100 см
4.2.13 Йод (применяется по выбору пользователя), раствор концентрацией
4.2.14 Кислота серная, раствор концентрацией
4.3 Стандартные вещества
4.3.1 Кислота аскорбиновая (L(+)-аскорбиновая) с массовой долей  (C
(C H
H O
O )
) 99,0%
99,0%
(R)-5-[(S)-1,2-дигидроксиэтил]-3,4-дигидрокси-5-Н-фуран-2-он.
4.3.2 Кислота изоаскорбиновая (D(-)-аскорбиновая) с массовой долей (C
(C H
H O
O )
) 99,0%
99,0%
(R)-5-[(R)-1,2-дигидроксиэтил]-3,4-дигидрокси-5-Н-фуран-2-он.
(R)-5-[(S)-1,2-дигидроксиэтил]-3,4-дигидрокси-5-Н-фуран-2-он.
4.3.2 Кислота изоаскорбиновая (D(-)-аскорбиновая) с массовой долей
(R)-5-[(R)-1,2-дигидроксиэтил]-3,4-дигидрокси-5-Н-фуран-2-он.
4.4 Основные стандартные растворы
4.4.1 Основной стандартный раствор аскорбиновой кислоты с массовой концентрацией  (С
(С Н
Н O
O )=1 мг/см
)=1 мг/см
100 мг аскорбиновой кислоты (см. 4.3.1), измеренной с точностью до 0,1 мг, растворяют в определенном объеме (например, 100 см ) раствора метафосфорной кислоты (см. 4.2.8). Раствор готовят в день проведения анализа.
) раствора метафосфорной кислоты (см. 4.2.8). Раствор готовят в день проведения анализа.
Стабильность основного раствора аскорбиновой кислоты может быть повышена добавлением L-цистеина.
4.4.2 Основной стандартный раствор изоаскорбиновой кислоты с массовой концентрацией (С
(С Н
Н O
O )=1 мг/см
)=1 мг/см
100 мг изоаскорбиновой кислоты (см. 4.3.2), измеренной с точностью до 0,1 мг, растворяют в определенном объеме (например, 100 мл) раствора метафосфорной кислоты (см. 4.2.8). Раствор готовят в день проведения анализа.
4.4.3 Проверка концентрации основного стандартного раствора (выполняется по выбору пользователя)
Около 150 мг аскорбиновой кислоты помещают в колбу Эрленмейера, добавляют 10 см раствора серной кислоты (см. 4.2.14) и 80 см
раствора серной кислоты (см. 4.2.14) и 80 см воды, не содержащей диоксида углерода, содержимое колбы перемешивают до полного растворения аскорбиновой кислоты. После добавления раствора крахмала (см. 4.2.12) полученный раствор титруют раствором йода (см. 4.2.13) до появления устойчивой синей окраски. Масса аскорбиновой кислоты, эквивалентная 1 см
воды, не содержащей диоксида углерода, содержимое колбы перемешивают до полного растворения аскорбиновой кислоты. После добавления раствора крахмала (см. 4.2.12) полученный раствор титруют раствором йода (см. 4.2.13) до появления устойчивой синей окраски. Масса аскорбиновой кислоты, эквивалентная 1 см раствора йода, пошедшего на титрование, составляет 8,81 мг.
раствора йода, пошедшего на титрование, составляет 8,81 мг.
Массовую долю основного компонента в стандартном веществе , %, вычисляют по формуле
, %, вычисляют по формуле
 , (1)где
, (1)где  - объем раствора йода, пошедший на титрование, см
- объем раствора йода, пошедший на титрование, см ;
;
8,81 - коэффициент пересчета;
100 - коэффициент пересчета результата в процентное содержание;
 - масса навески стандартного вещества, мг
- масса навески стандартного вещества, мг
100 мг аскорбиновой кислоты (см. 4.3.1), измеренной с точностью до 0,1 мг, растворяют в определенном объеме (например, 100 см
Стабильность основного раствора аскорбиновой кислоты может быть повышена добавлением L-цистеина.
4.4.2 Основной стандартный раствор изоаскорбиновой кислоты с массовой концентрацией
100 мг изоаскорбиновой кислоты (см. 4.3.2), измеренной с точностью до 0,1 мг, растворяют в определенном объеме (например, 100 мл) раствора метафосфорной кислоты (см. 4.2.8). Раствор готовят в день проведения анализа.
4.4.3 Проверка концентрации основного стандартного раствора (выполняется по выбору пользователя)
Около 150 мг аскорбиновой кислоты помещают в колбу Эрленмейера, добавляют 10 см
Массовую долю основного компонента в стандартном веществе
8,81 - коэффициент пересчета;
100 - коэффициент пересчета результата в процентное содержание;
4.5 Градуировочные растворы
4.5.1 Градуировочные растворы аскорбиновой кислоты массовыми концентрациями  (С
(С Н
Н O
O )=5-50 мкг/см
)=5-50 мкг/см
От 0,5 до 5,0 см основного раствора аскорбиновой кислоты (см. 4.4.1) переносят пипеткой в мерные колбы вместимостью 100 см
основного раствора аскорбиновой кислоты (см. 4.4.1) переносят пипеткой в мерные колбы вместимостью 100 см , объем содержимого в колбах доводят до метки раствором метафосфорной кислоты (см. 4.2.8). Растворы готовят в день проведения анализа.
, объем содержимого в колбах доводят до метки раствором метафосфорной кислоты (см. 4.2.8). Растворы готовят в день проведения анализа.
От 0,5 до 5,0 см
4.5.2 Градуировочный раствор изоаскорбиновой кислоты с массовой концентрацией  (С
(С Н
Н O
O )=10 мкг/см
)=10 мкг/см
1 см основного раствора изоаскорбиновой кислоты (см. 4.4.2) переносят пипеткой в мерную колбу вместимостью 100 см
основного раствора изоаскорбиновой кислоты (см. 4.4.2) переносят пипеткой в мерную колбу вместимостью 100 см , объем содержимого доводят до метки раствором метафосфорной кислоты (см. 4.2.8). Раствор готовят в день проведения анализа.
, объем содержимого доводят до метки раствором метафосфорной кислоты (см. 4.2.8). Раствор готовят в день проведения анализа.
1 см
5 Приборы и оборудование
5.1 Общие положения
Для проведения испытаний используют лабораторные приборы, лабораторную посуду и оборудование из стекла, в частности перечисленные ниже.
5.2 Спектрофотометр с рабочим спектральным диапазоном в ультрафиолетовой области, пригодный для измерения оптической плотности при приведенных ниже длинах волн.
5.3 Жидкостный хроматограф
Система для ВЭЖХ, состоящая из насоса, устройства ввода пробы, спектрофотометрического детектора, пригодного для измерения оптической плотности при длине волны 265 нм, и системы сбора и обработки данных, например интегратора.
5.4 Колонка для ВЭЖХ-анализа
5.4.1 Общие положения
Критерием пригодности колонки является разделение пиков L-аскорбиновой и изоаскорбиновой кислот на уровне базовой линии [3].
Критерием пригодности колонки является разделение пиков L-аскорбиновой и изоаскорбиновой кислот на уровне базовой линии [3].
5.4.2 Параметры хроматографической колонки
Колонка с внутренним диаметром 4,0 мм, длиной 250 мм, заполненная обращенно-фазовым сорбентом на основе силикагеля с привитыми октадецильными группами и блокированными остаточными силанольными группами размером частиц сорбента 5 мкм.
Допустимо использовать колонку с другими размерами частиц сорбента или размерами колонки, чем те, что указаны в настоящем стандарте.
Колонка с внутренним диаметром 4,0 мм, длиной 250 мм, заполненная обращенно-фазовым сорбентом на основе силикагеля с привитыми октадецильными группами и блокированными остаточными силанольными группами размером частиц сорбента 5 мкм.
Допустимо использовать колонку с другими размерами частиц сорбента или размерами колонки, чем те, что указаны в настоящем стандарте.
5.5 Устройство для фильтрации
Фильтрование подвижной фазы и раствора пробы перед использованием или вводом в хроматограф через мембранный фильтр размером пор, например 0,2 или 0,4 мкм, продлевает срок службы колонки.
6 Процедура проведения испытания
6.1 Общие положения
При проведении испытания обеспечивают предельно короткий промежуток времени между приготовлением растворов проб и градуировочных растворов и их анализом. Температура в помещении при проведении анализа не должна превышать 25 °С. Предельный срок использования анализируемых растворов - 8 ч с момента их приготовления.
6.2 Подготовка пробы
Исследуемую пробу гомогенизируют. Если проба представляет собой продукт твердой консистенции, ее измельчают на мельнице подходящей конструкции и снова тщательно перемешивают. Анализ пробы проводят непосредственно после ее гомогенизации. Подготовку к анализу проб свежих фруктов и овощей проводят одновременно с экстракцией (см. 6.3.1).
6.3 Приготовление раствора пробы для анализа
6.3.1 Экстракция
Навеску пробы массой, например, 3 г (при содержании витамина С в пробе около 50 мг/100 г), измеренной с точностью до 1 мг, помещают в мерную колбу вместимостью 100 см , добавляют 80 см
, добавляют 80 см раствора метафосфорной кислоты (см. 4.2.8), тщательно перемешивают, после чего объем в колбе доводят до метки. Содержимое колбы снова перемешивают, после чего фильтруют. Полученный раствор представляет собой экстракт из пробы.
раствора метафосфорной кислоты (см. 4.2.8), тщательно перемешивают, после чего объем в колбе доводят до метки. Содержимое колбы снова перемешивают, после чего фильтруют. Полученный раствор представляет собой экстракт из пробы.
При анализе свежих фруктов и овощей от 2 до 10 г измельченной ножом пробы помещают в стакан вместимостью 100 см , затем вносят некоторое количество раствора метафосфорной кислоты (см. 4.2.8).Содержимое стакана гомогенизируют, количественно переносят в мерную колбу вместимостью 100 см
, затем вносят некоторое количество раствора метафосфорной кислоты (см. 4.2.8).Содержимое стакана гомогенизируют, количественно переносят в мерную колбу вместимостью 100 см , перемешивают и фильтруют. Полученный раствор представляет собой экстракт из пробы.
, перемешивают и фильтруют. Полученный раствор представляет собой экстракт из пробы.
Примечание - Стабильность аскорбиновой кислоты в растворе можно повысить, например, путем добавления к раствору метафосфорной кислоты 125 см раствора L-цистеина (см. 4.2.10), дитиотрейтола или диэтилтиаминфосфорной кислоты. При этом следует иметь в виду, что эти стабилизаторы могут влиять на качество хроматографического разделения. Данная процедура не была использована при проведении межлабораторных испытаний.
раствора L-цистеина (см. 4.2.10), дитиотрейтола или диэтилтиаминфосфорной кислоты. При этом следует иметь в виду, что эти стабилизаторы могут влиять на качество хроматографического разделения. Данная процедура не была использована при проведении межлабораторных испытаний.
6.3.2 Проведение реакции восстановления
Аликвоту отфильтрованного экстракта (см. 6.3.1) объемом 20 см переносят в стакан вместимостью 50 см
переносят в стакан вместимостью 50 см ,
,
Навеску пробы массой, например, 3 г (при содержании витамина С в пробе около 50 мг/100 г), измеренной с точностью до 1 мг, помещают в мерную колбу вместимостью 100 см
При анализе свежих фруктов и овощей от 2 до 10 г измельченной ножом пробы помещают в стакан вместимостью 100 см
Примечание - Стабильность аскорбиновой кислоты в растворе можно повысить, например, путем добавления к раствору метафосфорной кислоты 125 см
6.3.2 Проведение реакции восстановления
Аликвоту отфильтрованного экстракта (см. 6.3.1) объемом 20 см
добавляют 10 см раствора L(+)-цистеина. Значение рН полученного раствора доводят до 7,0-7,2 при измерении с помощью рН-метра путем добавления по каплям раствора тринатрийфосфата (см. 4.2.9) при постоянном перемешивании с помощью магнитной мешалки. По достижении указанного значения рН раствор выдерживают точно 5 мин при постоянном перемешивании. По истечении указанного времени значение рН раствора доводят до 2,5-2,8 (по рН-метру) путем добавления по каплям раствора метафосфорной кислоты (см. 4.2.7) при постоянном перемешивании. Полученный раствор количественно переносят в мерную колбу вместимостью 50 см
раствора L(+)-цистеина. Значение рН полученного раствора доводят до 7,0-7,2 при измерении с помощью рН-метра путем добавления по каплям раствора тринатрийфосфата (см. 4.2.9) при постоянном перемешивании с помощью магнитной мешалки. По достижении указанного значения рН раствор выдерживают точно 5 мин при постоянном перемешивании. По истечении указанного времени значение рН раствора доводят до 2,5-2,8 (по рН-метру) путем добавления по каплям раствора метафосфорной кислоты (см. 4.2.7) при постоянном перемешивании. Полученный раствор количественно переносят в мерную колбу вместимостью 50 см , при этом электроды рН-метра, рабочий элемент магнитной мешалки и стакан, в котором находился раствор, ополаскивают водой, перенося смывы в ту же колбу. Объем содержимого в мерной колбе доводят до метки водой, содержимое колбы перемешивают. Полученный раствор фильтруют через мембранный фильтр (см. 5.5), фильтрат используют для хроматографического анализа.
, при этом электроды рН-метра, рабочий элемент магнитной мешалки и стакан, в котором находился раствор, ополаскивают водой, перенося смывы в ту же колбу. Объем содержимого в мерной колбе доводят до метки водой, содержимое колбы перемешивают. Полученный раствор фильтруют через мембранный фильтр (см. 5.5), фильтрат используют для хроматографического анализа.
При наличии информации о присутствии в анализируемом продукте добавок-загустителей рекомендуется их удалить из анализируемого раствора перед его хроматографическим анализом во избежание порчи хроматографической колонки. Для этого к порции восстановленного раствора пробы объемом 4 см добавляют 1 см
добавляют 1 см метанола (см. 4.2.6), полученный раствор перемешивают и фильтруют через мембранный фильтр (см. 5.5). Фильтрат используют для хроматографического анализа.
метанола (см. 4.2.6), полученный раствор перемешивают и фильтруют через мембранный фильтр (см. 5.5). Фильтрат используют для хроматографического анализа.
При наличии информации о присутствии в анализируемом продукте добавок-загустителей рекомендуется их удалить из анализируемого раствора перед его хроматографическим анализом во избежание порчи хроматографической колонки. Для этого к порции восстановленного раствора пробы объемом 4 см
6.4 Идентификация
Пик L-аскорбиновой кислоты на хроматограмме раствора пробы идентифицируют по совпадению его времени удерживания со временем удерживания пика аналита на хроматограмме градуировочного раствора, полученной при тех же параметрах хроматографического анализа. Идентификацию пика аналита можно также проводить путем добавления стандартного раствора в раствор пробы.
Ниже приведены параметры хроматографического анализа, обеспечивающие требуемую степень хроматографического разделения и пригодные для количественного определения (см. также рисунок А.1). Данные параметры были использованы при проведении межлабораторных испытаний.
Параметры хроматографической колонки: колонка, заполненная обращенно-фазовым сорбентом на основе силикагеля с привитыми октадецильными группами и блокированными остаточными силанольными группами размером частиц сорбента 5 мкм, длина колонки 250 мм, внутренний диаметр 4,0 мм;
Ниже приведены параметры хроматографического анализа, обеспечивающие требуемую степень хроматографического разделения и пригодные для количественного определения (см. также рисунок А.1). Данные параметры были использованы при проведении межлабораторных испытаний.
Параметры хроматографической колонки: колонка, заполненная обращенно-фазовым сорбентом на основе силикагеля с привитыми октадецильными группами и блокированными остаточными силанольными группами размером частиц сорбента 5 мкм, длина колонки 250 мм, внутренний диаметр 4,0 мм;
| подвижная фаза | смесь раствора А и раствора В (4.2.11); | |||
| скорость потока подвижной фазы | 0,7 см | |||
| ижектируемый объем | 30 мм | |||
| длина волны детектирования | 265 нм. | |||
